高中 | 氧化还原反应方程式的书写及配平 题目答案及解析
稿件来源:高途
高中 | 氧化还原反应方程式的书写及配平题目答案及解析如下,仅供参考!
必修一
第二章 化学物质及其变化
第三节 氧化还原反应
氧化还原反应方程式的书写及配平
氯化铬四氢呋喃复合物是一种配位化合物,化学式为$\text{CrC}{{\text{l}}_{3}}\cdot {{\left( \text{THF} \right)}_{3}}$,在有机合成反应中作催化剂。
已知:①$\text{CrC}{{\text{l}}_{3}}$易潮解,易升华,高温下易被氧气氧化;②$\text{COC}{{\text{l}}_{2}}$气体有毒,遇水发生水解产生两种酸性气体;③$\text{CrC}{{\text{l}}_{3}}\cdot {{\left( \text{THF} \right)}_{3}}$的摩尔质量为$374.5\;\rm{ g\cdot mo}{{\text{l}}^{-1}}$;④四氢呋喃$\rm (THF)$的结构简式为![]() ,易挥发,高度易燃。
,易挥发,高度易燃。
Ⅰ.制备无水$\text{CrC}{{\text{l}}_{3}}$
某化学小组用$\text{C}{{\text{r}}_{2}}{{\text{O}}_{3}}$和$\text{CC}{{\text{l}}_{4}}\rm ($沸点$76.8\;^\circ \rm C \rm )$在高温下制备无水$\text{CrC}{{\text{l}}_{3}}$,同时生成$\text{COC}{{\text{l}}_{2}}$,气体,实验装置如图所示:
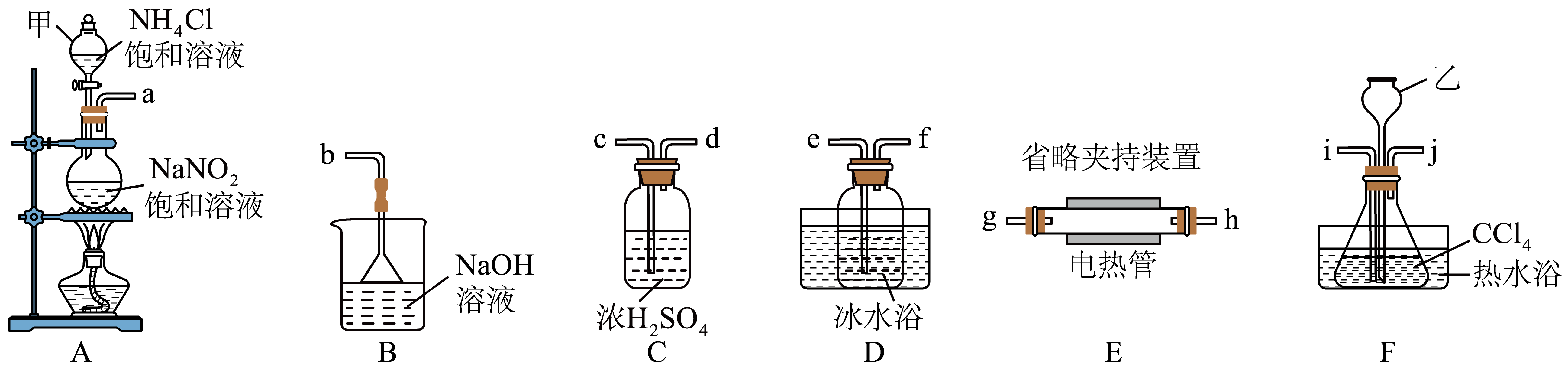
实验装置合理的连接顺序为$\rm a→$ $\rm →c→d→b($填装置接口标号,可重复使用$\rm )$。
$\\rm c→d→i→j→g→h→e→f(g$、$\\rm h$可换顺序$\\rm )$
"]]由分析知,实验装置合理的连接顺序为$\rm a→c→d→i→j→g→h→e→f(g$、$\rm h$可换顺序$\rm )→c→d→b$。
仪器乙的名称为 ,作用是 。
长颈漏斗;平衡压强
"]]乙的名称为长颈漏斗;作用是平衡压强,防止装置堵塞。
尾气处理时发生反应的离子方程式为 。
$\\text{COC}{{\\text{l}}_{2}}+4\\text{O}{{\\text{H}}^{-}}=\\text{CO}_{3}^{2-}+2\\text{C}{{\\text{l}}^{-}}+2{{\\text{H}}_{2}}\\text{O}$
"]]尾气处理时,$\rm NaOH$溶液与$\text{COC}{{\text{l}}_{2}}$发生反应生成碳酸钠和氯化钠,离子方程式为$\text{COC}{{\text{l}}_{2}}+4\text{O}{{\text{H}}^{-}}=\text{CO}_{3}^{2-}+2\text{C}{{\text{l}}^{-}}+2{{\text{H}}_{2}}\text{O}$。
Ⅱ.合成$\text{CrC}{{\text{l}}_{3}}\cdot {{\left( \text{THF} \right)}_{3}}$
②实验室在非水体系中合成$\text{CrC}{{\text{l}}_{3}}\cdot {{\left( \text{THF} \right)}_{3}}$的原理为$\text{CrC}{{\text{l}}_{3}}+3\text{THF}\underset{\text{Zn}}{\overset{\triangle }{\mathop{\to }}}\,\text{CrC}{{\text{l}}_{3}}\cdot {{\left( \text{THF} \right)}_{3}}$
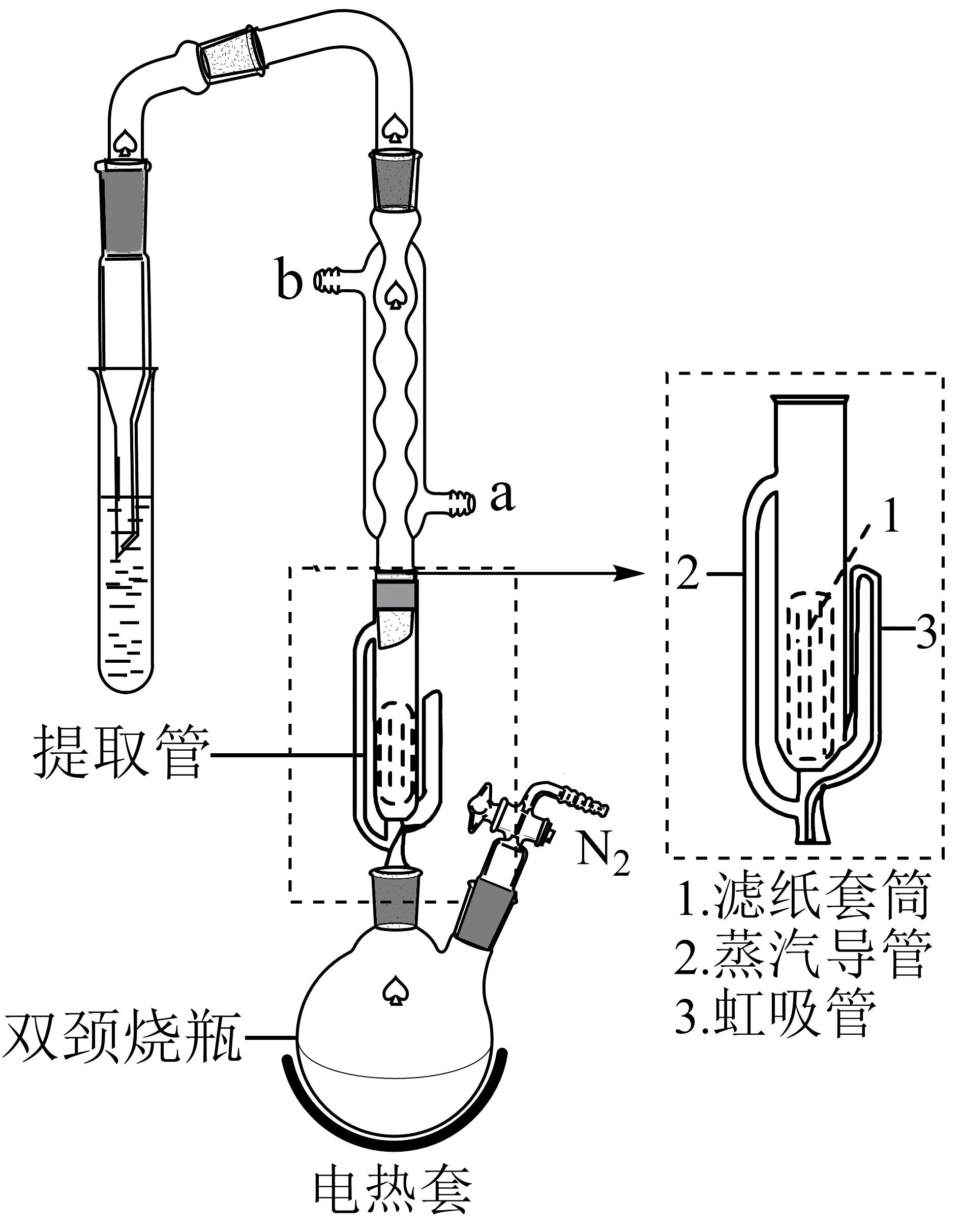
实验步骤:
①填装反应物:称取$\rm 4.755\;\rm g(0.03\;\rm mol)$无水$\text{CrC}{{\text{l}}_{3}}$和$\rm 0.20\;\rm g$锌粉放入滤纸套筒内,双颈烧瓶中加入$\rm 100\;\rm mL$无水$\rm THF($过量$\rm )$。
合成$\text{CrC}{{\text{l}}_{3}}\cdot {{\left( \text{THF} \right)}_{3}}$:先通入一段时间${{\text{N}}_{2}}$后,在球形冷凝管中通入冷却水,加热$\rm THF$至沸腾,$\rm THF$蒸气通过蒸气导管进入提取管中,在冷凝管中冷凝回流到滤纸套筒中进行反应,当滤纸套筒中的液面高于虹吸管最高处时,发生虹吸现象,滤纸套筒中的液体流入双颈峣瓶,从而实现了$\rm THF$与$\text{CrC}{{\text{l}}_{3}}$的连续反应及产物的连续萃取。
③分离$\text{CrC}{{\text{l}}_{3}}\cdot {{\left( \text{THF} \right)}_{3}}$:回流$\rm 2.5\;\rm h$,再通入${{\text{N}}_{2}}$冷却至室温。取下双颈烧瓶,在通风榐中蒸发$\rm THF$至有较多固体析出,冷却、抽滤、干燥称量,得产品$\rm 3.745\;\rm g$。
球形冷凝管进水口为 $\rm ($填“$a$”或“$b$”$\rm )$口。
$\\rm a$
"]]球形冷凝管冷凝水的方向为下进上出,故进水口为$\rm a$。
该实验不能使用明火加热的原因是 。
$\\rm THF$易挥发,高度易燃,遇明火可能发生爆炸
"]]由题中信息可知$\rm THF$沸点较低,且可以燃烧,故不可用明火直接加热的原因是$\rm THF$易挥发,易燃,遇明火可能发生爆炸。
已知$\rm Cr($Ⅱ$\rm )$对该反应有催化作用,推断加入少量$\rm Zn$粉发生反应的化学方程式为 。
$\\text{Zn}+2\\text{CrC}{{\\text{l}}_{3}}=2\\text{CrC}{{\\text{l}}_{2}}+\\text{ZnC}{{\\text{l}}_{2}}$
"]]加入锌可以把三价铬还原为二价铬,方程式为:$\text{Zn}+2\text{CrC}{{\text{l}}_{3}}=2\text{CrC}{{\text{l}}_{2}}+\text{ZnC}{{\text{l}}_{2}}$。
产品产率为 。$\rm ($结果保留$\rm 3$位有效数字$\rm )$
$33.3\\%\\rm ($答“$0.333\\sim 0.340$”均可$\\rm )$
"]]由题目中的信息可知如下对应关系式:$\begin{matrix} \text{CrC}{{\text{l}}_{3}} & + & 3\text{THF} & \underset{\text{Zn}}{\overset{\triangle }{\mathop{\to }}}\, & \text{CrC}{{\text{l}}_{3}}\cdot {{\left( \text{THF} \right)}_{3}} \\ 158.8 & {} & {} & {} & 374.5 \\ 4.755 & {} & {} & {} & {x} \\ \end{matrix}$,$x=\dfrac{374.5\times 4.755\text{ g}}{158.8}=11.235\text{ g}$,产率为$\dfrac{\text{3}\text{.745 g}}{\text{11}\text{.235 g}}\times100\%=33.3\%$。
高中 | 氧化还原反应方程式的书写及配平题目答案及解析(完整版)
