高中 | 杂化轨道理论 题目答案及解析
稿件来源:高途
高中 | 杂化轨道理论题目答案及解析如下,仅供参考!
选修三
第二章 分子结构与性质
第二节 分子的立体结构
杂化轨道理论
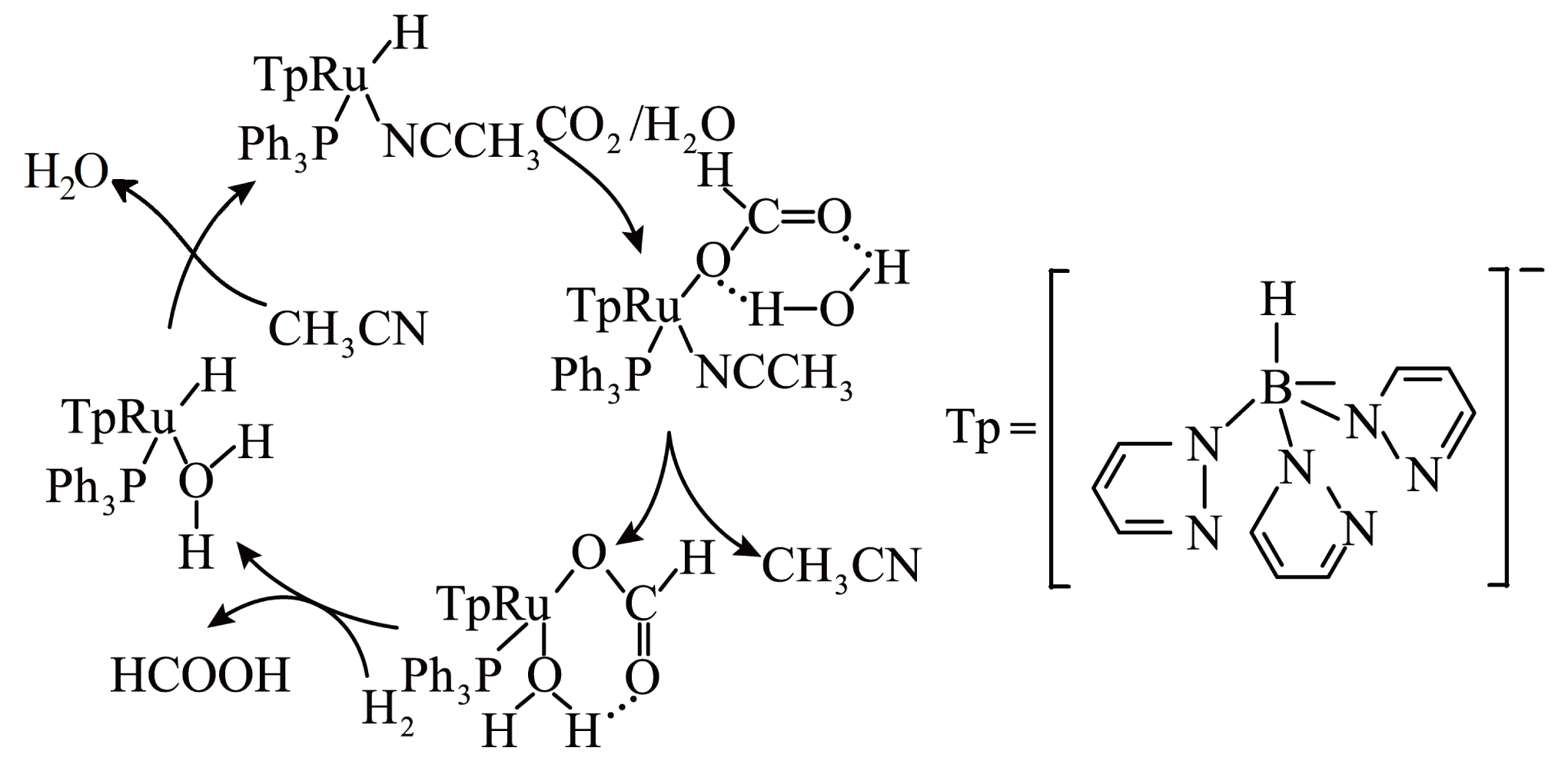
含$\rm Tp$配体的钌$\rm (Ru)$配合物催化氢化$\text{C}{{\text{O}}_{2}}$生成甲酸的机理如图所示。下列叙述错误的是$(\qquad)$
![]()
["
循环$\\rm A$中$\\rm Ru$的成键数目不变
","循环$\\rm A$中物质所含氢键均为分子间氢键
","图中涉及的$\\rm CH_{3}CN$和$\\rm HCOOH$,碳原子有三种杂化方式
","该催化反应的原子利用率为$\\rm 100\\%$
"][["B"]]
$\rm A$.从图中可知,循环中$\rm Ru$的成键数目一直为$\rm 4$,没有变化,故$\rm A$正确;
$\rm B$.从图中可知,循环图右上方的物质与水分子形成分子间氢键,右下方的物质形成分子内氢键,故$\rm B$错误;
$\rm C$.$\rm CH_{3}CN$和$\rm HCOOH$中存在$\rm -CH_{3}$、$\rm -COOH$和$\rm -C≡N$,碳原子有$\rm sp^{3}$、$\rm sp^{2}$、$\rm sp$三种杂化方式,故$\rm C$正确;
$\rm D$.从图中可知,该过程的总反应为$\text{C}{{\text{O}}_{2}}\rm +H_{2}=HCOOH$,是化合反应,原子利用率为$\rm 100\%$,故$\rm D$正确。
故选:$\rm B$
高中 | 杂化轨道理论题目答案及解析(完整版)
去刷题
今日推荐 ![]()
![]()
![]()
